Последние новости науки
Sunday, 14 April,

Saturday, 13 April,

Friday, 12 April,

Наука в блогах

Заоконье, 8 этаж / prokhozhyj.livejournal.com
Телевизор.+8 °C

С серединой весны! / don-beaver.livejournal.com
Понедельник был таким веселым, что не успел поздравить вас, друзья, с новым рубежом! Зато сегодня —...

"Птичьи дети" / prokhozhyj.livejournal.com
Тут днями вышла книжка, которую я хотел очень давно – с тех пор, как года четыре назад Игорь Белый прочитал в "Гиперионе" три главки "из пишущегося"....

Заоконье, 8 этаж / prokhozhyj.livejournal.com
"Ну, предположим, чирик?"+12 °C
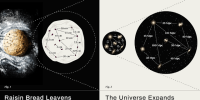
Результаты праймериз Демократической партии США за рубежом / kireev.livejournal.com
Результаты праймериз Демократической партии США за рубежом. Даже два варианты карты есть!ИсточникИсточникНекоторые намеки на систему есть, но на самом деле...

Melancholy Ecstatic Dance — новый мистический проект Ивана Никто / greenword.ru
В конце марта мастер-диджей Иникто (Иван Никто) провёл мероприятие Melancholy Ecstatic Dance в укромном особняке Бульварного кольца. Оно было приурочено к празднованию...